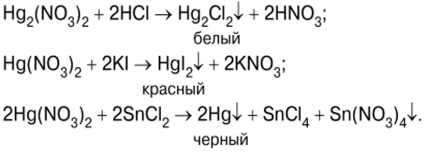
수은 화합물의 반응
금속성 수은과 그 화합물은 살아있는 유기체에 매우 유독합니다. 이것은 물에 잘 녹는 화합물에 특히 해당됩니다. 이 독특한 원소의 조합을 실험할 때는 각별한 주의가 필요합니다(수은은 실온에서 액체인 유일한 금속입니다). 화학자의 기본 수칙 준수? 수은 화합물로 여러 실험을 안전하게 수행할 수 있습니다.
첫 번째 실험에서 우리는 알루미늄 아말감(이 금속을 액체 수은에 녹인 용액)을 얻습니다. 수은(II) 용액 Hg 질산염(V) Hg(NO3)2 및 알루미늄 와이어 조각(사진 1). 알루미늄 막대(침전물을 조심스럽게 청소)를 용해성 수은염 용액이 포함된 시험관에 넣습니다(사진 2). 잠시 후 와이어 표면에서 기포가 방출되는 것을 관찰할 수 있습니다(사진 3 및 4). 용액에서 막대를 제거한 후 점토가 푹신한 코팅으로 덮여 있고 또한 금속 수은 공도 보입니다 (사진 5 및 6).
화학 - 수은 결합 경험
정상적인 조건에서 알루미늄의 표면은 산화알루미늄의 밀착된 층으로 코팅됩니다.2O3공격적인 환경 영향으로부터 금속을 효과적으로 분리합니다. 막대를 세척하고 수은염 용액에 담그면 Hg 이온이 치환됩니다.2+ 더 활동적인 알루미늄
막대 표면에 부착된 수은은 알루미늄과 아말감을 형성하여 산화물이 부착되기 어렵게 합니다. 알루미늄은 매우 활동적인 금속(물과 반응하여 수소를 방출 - 기포가 관찰됨)이며, 조밀한 산화물 코팅으로 인해 구조재로 사용이 가능합니다.
두 번째 실험에서는 암모늄 NH 이온을 검출합니다.4+ Nessler의 시약 사용(독일 화학자 Julius Nessler는 1856년 분석에 처음으로 사용했습니다).
홉과 수은 화합물의 반응 실험
테스트는 mercury(II) iodide HgI의 침전으로 시작됩니다.2, 요오드화칼륨 KI 및 수은(II) 질산(V) Hg(NO3)2 (사진 7):
HgI의 주황색-적색 침전물2 (사진 8) 그런 다음 과량의 요오드화 칼륨 용액으로 처리하여 화학식 K의 가용성 복합 화합물을 얻습니다.2HGI4 ? Nessler 시약인 Potassium tetraiodercurate(II)(사진 9):
생성된 화합물로 암모늄 이온을 감지할 수 있습니다. 수산화나트륨 NaOH 및 염화암모늄 NH 용액이 여전히 필요합니다.4Cl (사진 10). Nessler 시약에 소량의 암모늄염용액을 가하고 강염기로 매질을 알칼리화한 후 시험관 내용물이 황색-주황색으로 변하는 것을 관찰하였다. 현재 반응은 다음과 같이 쓸 수 있습니다.
생성된 수은 화합물은 다음과 같은 복잡한 구조를 갖습니다.
매우 민감한 Nessler 테스트는 물(예: 수돗물)에서 미량의 암모늄 염 또는 암모니아를 검출하는 데 사용됩니다.

