|
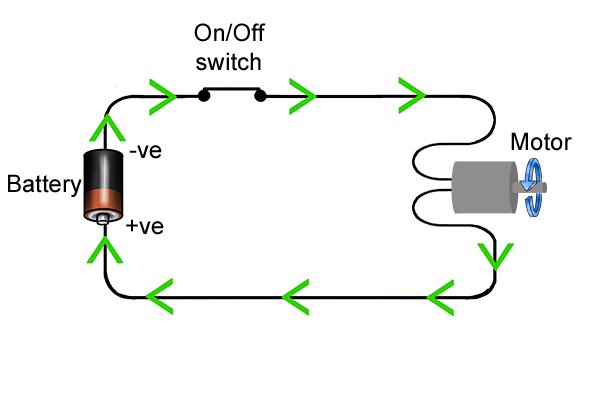
 | 배터리는 에너지를 저장했다가 전기 회로가 완성되면 방출하는 방식으로 작동합니다. 에너지를 활용하여 빛, 열 또는 움직임을 생성하는 데 사용할 수 있습니다. 이 에너지를 흔히 전기라고 합니다. |
 | 무선 전동 공구의 전원 버튼을 누르면 예를 들어 배터리에서 공구로 전원이 흐르고 드릴이 회전하는 전기 회로가 완성됩니다. |
 | 배터리는 제한된 양의 에너지만 저장할 수 있으며, 다 소모되면 충전기로 충전해야 합니다. 충전기는 주전원의 전기를 사용하여 배터리에 에너지를 보충하고 다시 사용할 준비가 됩니다. |
 | 모든 것을 작동시키는 화학에 관심이 있다면 계속 읽으십시오! |
배터리 화학 |
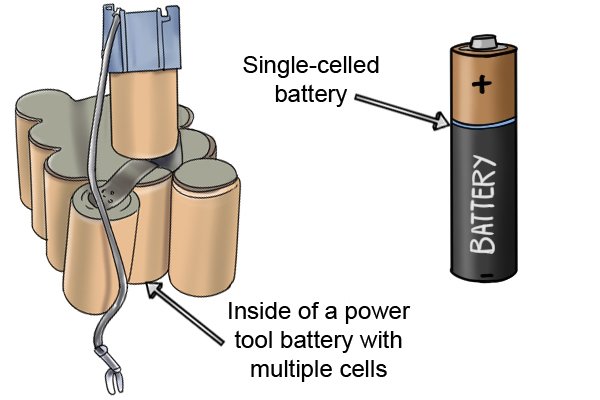
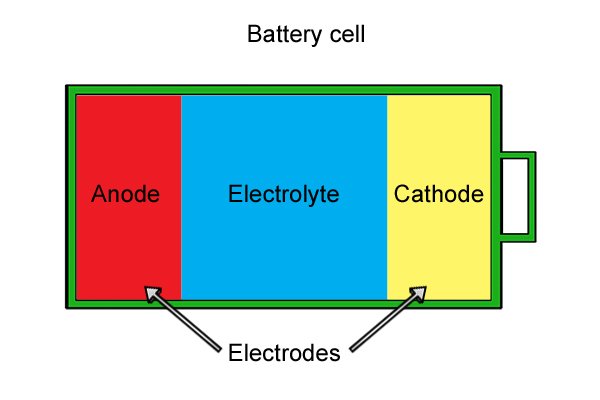
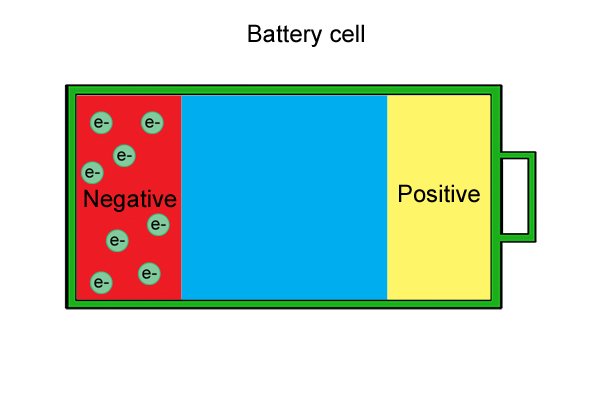
 | 무선 전동 공구용으로 설계된 배터리는 여러 배터리 "셀"로 구성되며 배터리 팩으로 알려져 있습니다. 셀이 많을수록 배터리가 소진되기 전에 더 많은 일을 할 수 있습니다. |
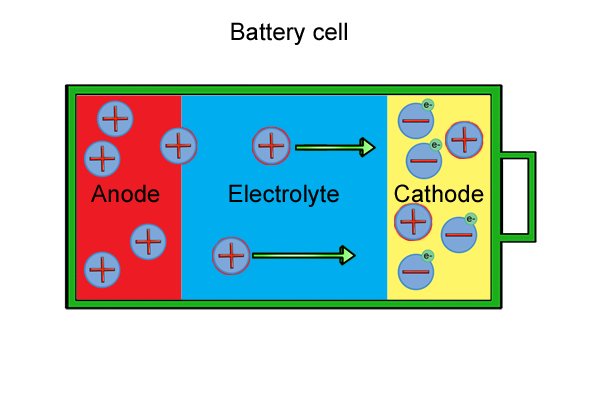
 | 각 셀 내부에는 양극, 음극 및 전해질이 있습니다. 집합적으로 "전극"으로 알려진 양극과 음극은 함께 놓을 때 반응하는 재료로 만들어집니다. 전해질은 전극을 서로 분리하는 액체 또는 젖은 페이스트입니다. |
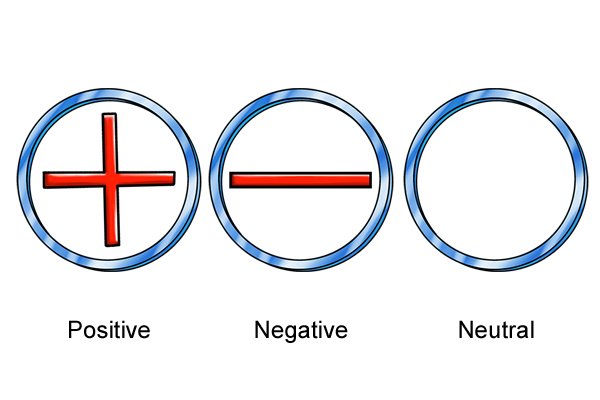
 | 세상의 모든 것은 전하(양, 음 또는 중성)에 따라 상호 작용하는 작은 분자로 구성됩니다. 배터리를 이해하려면 전극의 분자가 서로 어떻게 상호 작용하는지 살펴봐야 합니다. |
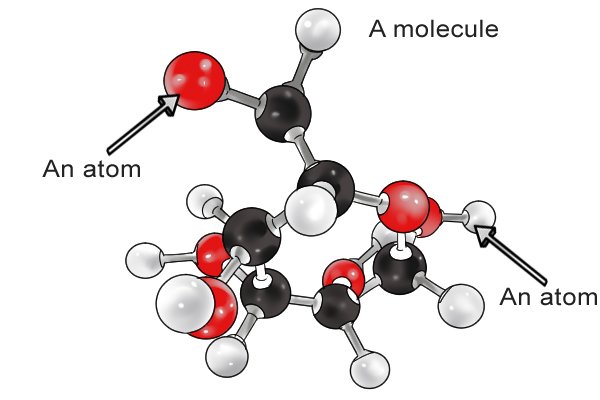
 | 분자는 가장 작은 빌딩 블록인 하나 이상의 원자로 구성됩니다. |
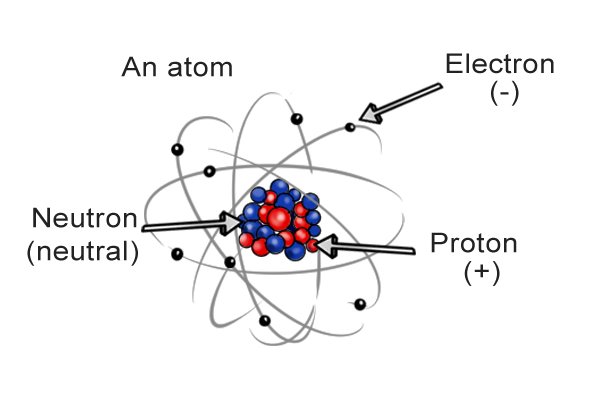
 | 각 원자는 그 중심에 중성자와 양성자를 포함하는 "핵"을 가지고 있습니다. 전자는 핵 주위를 돌고 있습니다. 중성자는 중성, 양성자는 양수, 전자는 음수입니다. 전하 사이의 균형은 원자의 총 전하를 결정하고 분자 내 원자 사이의 균형은 분자의 총 전하를 결정합니다. |
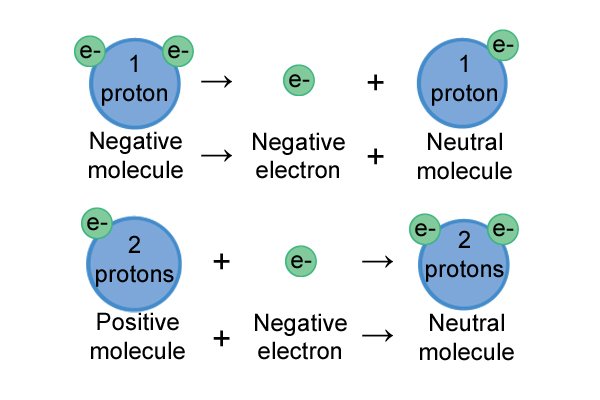
 | 모든 분자는 중립적이기를 원합니다. 그들이 이것을 할 수 있는 유일한 방법은 전자를 잃거나 얻는 것입니다. 양전하를 공유하면 전자를 끌어당기고 음전하를 공유하면 전자를 잃습니다. |
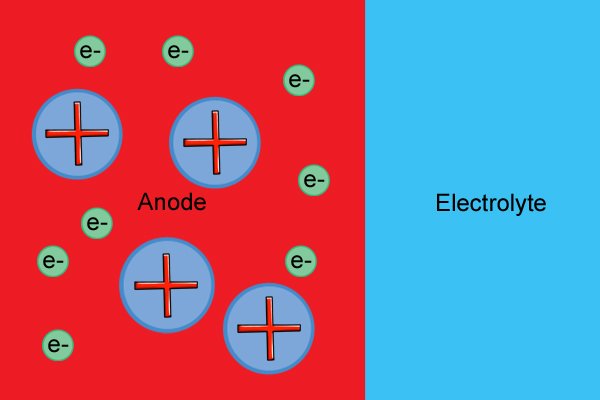
 | 양극 분자는 전자 방출("산화 반응"으로 알려짐) 및 양이온(하전된 분자) 형성을 유발하는 전해질과 반응할 때까지 중성입니다. |
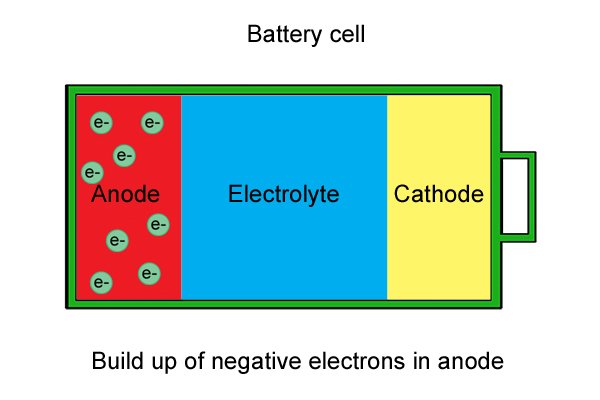
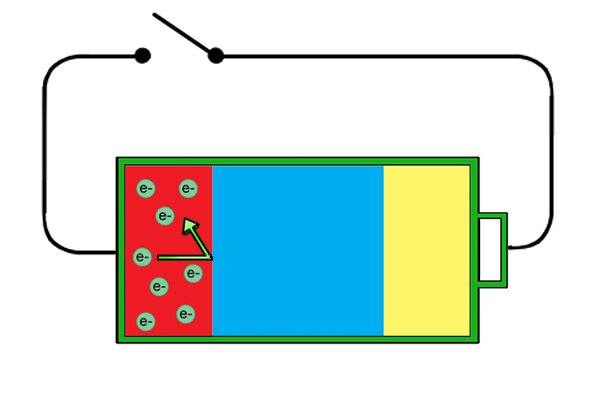
 | 이러한 "자유" 전자는 양극에 축적되어 음극이 됩니다. |
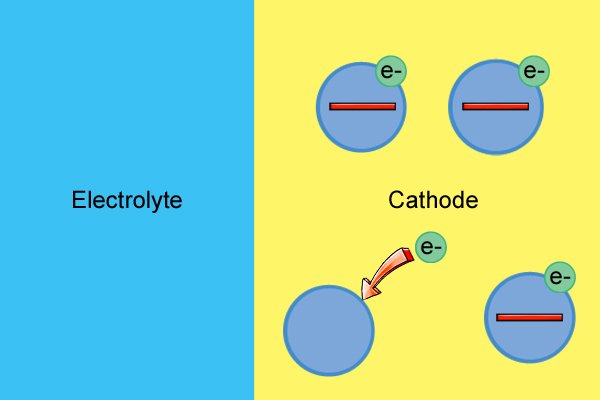
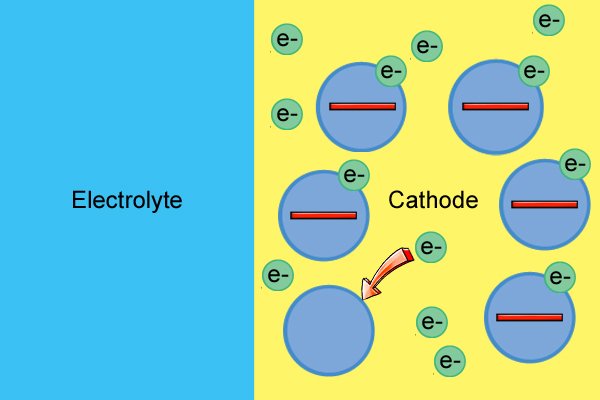
 | 음극 분자는 자유 전자를 사용하여 음이온을 형성하는(환원 반응으로 알려짐) 전해질과 반응할 때까지 중성입니다. |
 | 자유 전자의 소비는 음극이 더 이상 전자가 남지 않을 때까지 점점 더 양극이 되도록 합니다. |
 | 이제 양극은 전자를 밀어내고 음극은 전자를 요구하지만 회로가 불완전하면 양극의 자유 전자가 전해질을 통과하지 못하기 때문에 음극으로 갈 수 없습니다. |
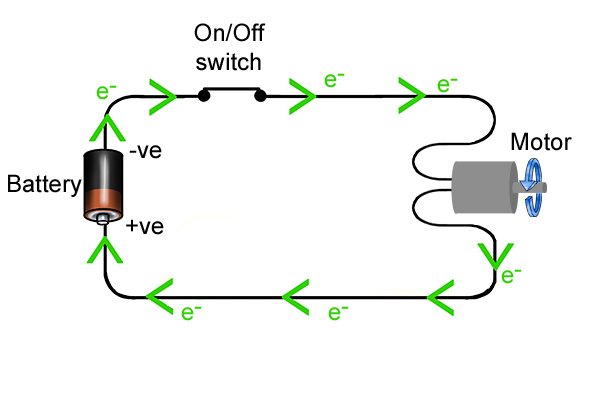
 | 회로가 완성되면 자유 전자가 전도체를 통해 양극에서 음극으로 흐를 수 있습니다. 그들이 도구를 통과할 때 그들이 운반하는 에너지는 무선 드릴에서 드릴을 돌리는 것과 같은 "작업"을 수행하는 데 사용될 수 있습니다. |
 | 음극에 도달하면 전자를 공급하여 환원 반응을 계속하고 전자가 추가됨에 따라 더 많은 음이온을 생성합니다. |
 | 한편, 양극에서는 전자의 손실로 인해 더 많은 양의 양이온이 형성되고, 이는 음극의 음이온에 끌리므로 양이온은 전해질을 통해 이동하기 시작하고 음극의 음이온과 혼합됩니다. . |
 | 모든 양이온이 음극으로 이동하고 더 이상 자유 전자가 남아 있지 않으면 배터리가 제대로 작동하지 않으므로 재충전해야 합니다. |
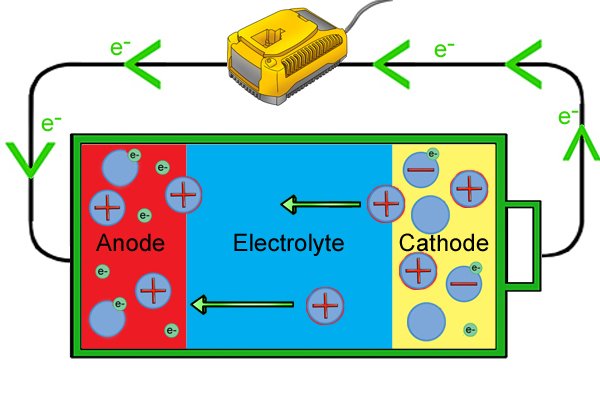
 | 충전기는 방전된 배터리를 통해 배터리 전압보다 높은 전압을 통과시킵니다. 이로 인해 배터리의 반응이 반전됩니다. |
 | 충전기에서 전기가 입력되면 음극의 전자가 회로를 통해 양극으로 되돌아갑니다. 모든 전자로 인해 양극이 더 음이 되면 양극의 양이온이 음극을 떠나기 시작하고 전해질을 통해 다시 양극으로 이동하여 자유 전자와 결합하여 다시 중성이 됩니다. |
 | 배터리가 다시 작동할 준비가 되었습니다! |